Скандал, связанный с индийской микстурой от кашля, заставил многие страны пересмотреть и ужесточить порядок допуска импортных лекарств на внутренние фармрынки. Редакция CMN.KZ выяснила, надёжно ли защищают казахстанцев от сомнительных препаратов и как обстоят дела у отечественной фарминдустрии
Надо отметить, что проблемы с медицинскими препаратами из Индии – частое явление последних лет. В частности, ВОЗ и власти разных стран (Узбекистана, Гамбии, Камеруна) связывали гибель десятков детей с приёмом определённых сиропов из этой страны, в которых обнаружили токсичные примеси – диэтиленгликоль и этиленгликоль.
Один из близких к нам случаев – 68 детских смертей в Узбекистане. Их зафиксировали с осени 2022 года по январь 2023-го. На выяснение причины, к сожалению, ушло немало времени. Оказалось, всему виной – приём препарата «Док-1 Макс» производства индийской фармкомпании Marion Biotech.
По сообщению Минздрава Узбекистана, в распространявшейся в стране партии лекарства был обнаружен этиленгликоль.
В ходе проверки всплыли и другие подробности: при проведении лабораторных исследований лекарства были грубо нарушены требования нормативно-правовой документации, в результате чего некачественный сироп допустили к продаже в стране. Так на судебном заседании сообщалось, что производитель препарата и его узбекские дистрибьюторы платили врачам и фармацевтам огромные суммы за то, чтобы те продвигали средство на местном рынке.
В итоге, помимо смертей, ещё 16 детей после такого «лечения» остались инвалидами.
К слову, в самой Индии осенью 2025 года приступили к расследованию по факту гибели девяти детей в штате Мадхья-Прадеш. Как выяснилось в ходе разбирательства, причиной смертей стал приём сиропа от кашля. В образцах партии данного препарата было обнаружено опасное содержание токсичного химического вещества.
Что сказали в ВОЗ и как отреагировал Казахстан
Сразу после резонанса Всемирная организация здравоохранения выпустила предупреждение об опасности трёх индийских сиропов от кашля.
Опасные компоненты, согласно данным, обнаружили в некоторых партиях Coldrif, Respifresh TR и ReLife, выпускаемых компаниями Sresan Pharmaceutical, Rednex Pharmaceuticals и Shape Pharma.
«В препаратах содержалось токсичное вещество диэтиленгликоль – растворитель, используемый в промышленных продуктах. В Coldrif его концентрация была близка к 50% при допустимой 0,1%», – говорилось в документе.
Производство на заводах компаний закрыли, а действие разрешений на продукцию приостановили.
В ВОЗ подчеркнули, что ни одно из опасных лекарств не экспортировалось из Индии, но призвали национальных регуляторов рассмотреть «возможность целевого надзора за рынком, уделяя особое внимание неформальным и нерегулируемым цепочкам поставок».
Между тем, как показал случай в Узбекистане, не всегда реализацию опасных препаратов удаётся остановить внутри страны-производителя. Как раз для этого и нужен тщательный контроль государств-импортёров.
В октябре 2025 года в Комитете медицинского и фармацевтического контроля Минздрава Казахстана прокомментировали информацию, связанную с сиропами из Индии и обращением ВОЗ.
В ведомстве заявили, что ни один из указанных трёх индийских препаратов от кашля не зарегистрирован в Казахстане и не имеет сертификатов соответствия. А стало быть, купить его легально на территории нашей страны невозможно.
Гражданам в очередной раз напомнили об осторожности и призвали приобретать лекарства только в лицензированных аптеках.
С аптечки – долой
Однако случаи, когда те или иные медицинские препараты в экстренном порядке изымают из аптечных сетей в нашей стране, нередки. То же можно сказать и о попытках нелегального ввоза лекарств и БАДов в Казахстан. За последние месяцы зарегистрировано уже несколько таких фактов.
Один из недавних инцидентов произошёл в конце марта 2026 года, когда в Алматы чуть не попали более тонны препаратов из Индии. Злоумышленники замаскировали их под косметику. Опасную подмену обнаружили сотрудники таможни аэропорта мегаполиса.


Как пояснили в Департаменте государственных доходов Алматы, согласно сопроводительным документам продукция числилась как косметические средства. На самом деле в коробках обнаружили 39 наименований лекарств. Нелегальную партию оценили более чем в пять миллионов тенге. При этом неизвестно, насколько эти препараты были безопасны.
Также в марте в стране запретили уже отечественный препарат – таблетки «Стрептоцид» производства казахстанской компании «Химфарм». Основанием для изъятия лекарства стало письмо Национального центра экспертизы лекарственных средств и медицинских изделий Комитета медицинского и фармацевтического контроля Минздраваот и протокол испытаний от 13 февраля 2026 года.
В конце февраля в Казахстане под запрет попало лекарство из Индии, но только из определённой серии. По приказу главы Комитета медицинского и фармацевтического контроля Минздрава его также изъяли из обращения.
Речь шла о таблетках «Десилмакс», которые помогают бороться с эректильной дисфункцией у мужчин. Позднее стало известно, что препарат отозвали из-за проблем с маркировкой, а именно – из-за несоответствия расположения надписи на упаковке.
Проверки и контроль
Чтобы узнать о том, кто в стране следит за безопасностью препаратов, попадающих в аптеки, а также, что входит в процедуру, предваряющую регистрацию того или иного лекарства на территории Казахстана, мы обратились с запросом в Министерство здравоохранения.

Как говорится в ответе ведомства, контроль за качеством препаратов в стране сосредоточен в руках государства. Руководством и реализацией в сферах медицинской и фармацевтической промышленности, а также контролем за обращением лекарственных средств и медицинских изделий, занимается Комитет медицинского и фармацевтического контроля.
Что касается непосредственно лекарств, то здесь ведущую роль играет Национальный центр экспертизы лекарственных средств и медицинских изделий (НЦЭЛС). Его специалисты проверяет продукцию на всех этапах – от регистрации до выхода на рынок и последующих лабораторных испытаний.
«Комитет является государственной экспертной организацией в сфере обращения лекарственных средств и медицинских изделий. Он занимается производственно-хозяйственной деятельностью в области здравоохранения по обеспечению безопасности, эффективности и качества лекарственных средств и медицинских изделий».
По сути, все вопросы, связанные с аккредитацией испытательных лабораторий, осуществляющих монопольную деятельность по экспертизе и оценке безопасности и качества лекарственных средств, а также медицинских изделий, также решает Комитет.
И здесь важный момент. Прежде чем препарат попадет в открытый доступ, проще говоря, на полки аптек, ему и его производителям предстоит пройти немало испытания. В частности, основные этапы включают в себя государственную регистрацию. Это самый важный документ, без него препарат нельзя продавать. И первый шаг в этом направлении – комплексная экспертиза.
Речь идёт о проверке всех документов. Это полная информация (почти паспорт) лекарства, результаты клинических испытаний, досье на производителя. Затем – лабораторные испытания. Здесь образцы препарата проверяют на соответствие заявленному составу, чистоте и эффективности. И если всё в порядке, то тогда его регистрируют, а затем вносят в государственный реестр. По факту после этого препарат можно ввозить в Казахстан и продавать. Но и здесь есть нюанс.

Несмотря на включение в госреестр, лекарства продолжают контролировать. Каждую партию, которую ввозят в страну обязательно проверяют прежде чем выпустить в продажу. Процесс включает в себя декларирование, выборочный контроль и сертификат соответствия.
Кроме того, с 2024 года в Казахстане действует обязательная маркировка на лекарства. Она помогает отслеживать весь путь товара и исключает попадание контрафакта в легальный оборот. Также действует и пострегистрационный контроль – мониторинг побочных эффектов и изъятие препарата из обращения, если возникают проблемы.
«Оценка качества лекарственных средств и медицинских изделий, зарегистрированных в Казахстане, проводится путем определения соответствия качества лекарственных средств и медицинских изделий данным регистрационного досье, нормативных документов по качеству лекарственных средств, на основании которых они были зарегистрированы в стране», – говорится также в ответе Минздрава.
Кроме того, экспертная организация ежегодно формирует план отбора образцов лекарственных средств и медицинских изделий, находящихся в обращении в Казахстане, для оценки качества.
«Испытания образцов продукции, отобранной с рынка, проводятся в испытательных лабораториях экспертной организации. При отрицательных результатах испытаний образцов продукции, отобранной с рынка, государственный орган принимает решение по приостановлению сертификата соответствия и изъятию из обращения лекарственного средства и медицинского изделия, не соответствующего требованиям законодательства».
Маркетплейсы тоже под прицелом. Их мониторинг проводится регулярно. В случае выявления продаж незарегистрированных лекарственных средств и медицинских изделий, как пояснили в Минздраве, Комитет направляет письмо в адрес площадок с требованием устранить нарушения.
Почему лекарство могут запретить?
Решение о приостановлении или запрете применения, реализации или производства лекарственных средств и медицинских изделий, а также об изъятии из обращения или ограничении применения принимают в случаях:
- несоответствия лекарственных средств и медицинских изделий требованиям законодательства в области здравоохранения;
- выявления нежелательных реакций, опасных для здоровья человека, не указанных в инструкции по медицинскому применению лекарственного средства, или повышения частоты выявления случаев серьезных нежелательных реакций, указанных в инструкции;
- при низкой терапевтической эффективности (отсутствие терапевтического эффекта);
- при наличии информации о приостановлении или отзыве препарата с рынка других стран в связи с выявлением серьезных нежелательных реакций с неблагоприятным соотношением «польза-риск»;
- нарушения утвержденного процесса производства лекарственных средств и медицинских изделий, влияющего на безопасность, качество и эффективность их применения;
- наличия данных о нанесении вреда здоровью пациента или потребителя в связи с применением лекарственных средств и медицинских изделий;
- получения данных о недостаточности научно-технического уровня технологии производства и контроля качества, обеспечивающих снижение уровня безопасности применения лекарственных средств и медицинских изделий;
- несоответствие лекарственных средств требованиям надлежащих фармацевтических практик Казахстана или Евразийского экономического союза, выявленного по результатам фармацевтической инспекции;
- невыполнения обязательств по фармаконадзору держателем регистрационного удостоверения лекарственного средства и производителем медицинского изделия по мониторингу безопасности, качества и эффективности медицинских изделий.
Решение о приостановлении продажи препарата принимают достаточно быстро – в течение трёх рабочих дней.
«Государственный орган в течение одного рабочего дня со дня принятия решения, извещает об этом в письменной форме территориальные подразделения, держателя регистрационного удостоверения лекарственных средств и медицинских изделий и экспертную организацию. Кроме того, данное решение размещается на официальных интернет-ресурсах Комитета и его Департаментов», – говорится в ответе Минздрава.
Побочные эффекты и нежелательные реакции: куда сообщать?
По каждому случаю выявления нежелательных реакций после того или иного лекарства, экспертная организация проводит анализ, изучает причинно-следственную связь между развитием этого состояния и приёмом препарата и даёт экспертное заключение.

Казахстанцы могут сообщить о нежелательных реакциях на лекарственные препараты следующим способом:
- прийти на приём к своему лечащему врачу или обратиться к фармацевту и сообщить о возникших побочных действиях;
- обратиться к уполномоченной организации, принимающей претензии по данной продукции, указанной в инструкциях лекарственных средств и медицинских изделий;
- через мобильное приложение «DariKZ» в раздел «Жёлтые карты», которое доступно для устройств на платформах iOS и Android. Там нужно заполнить сведения о пациенте и препарате, указать контактные данные для обратной связи и отправить сообщение. Информация поступит напрямую в Экспертную организацию.
Самые популярные лекарства и цены
Недавно в Минздраве рассказали о самых популярных лекарствах у казахстанцев. Составить список препаратов, которые покупают в стране чаще всего, помогла как раз маркировка. Поскольку система позволяет фиксировать потребительский спрос в режиме реального времени.
Получился вот такой рейтинг.
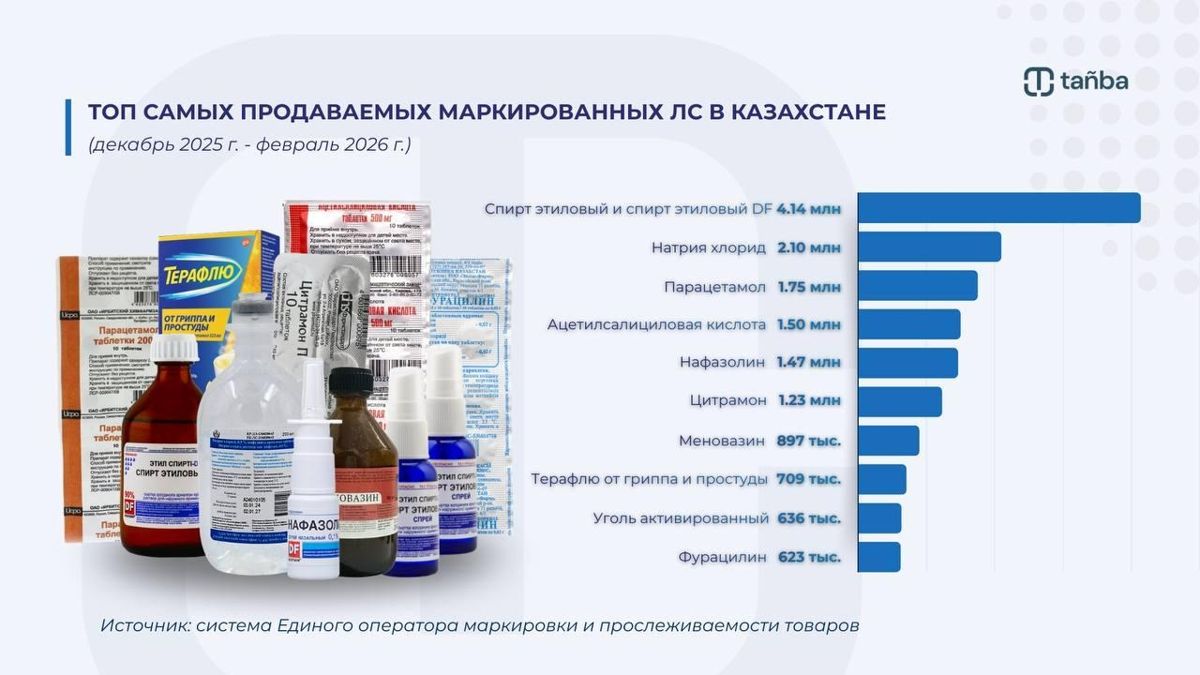
«Лидером продаж, как и в остальные времена года, стал этиловый спирт. Его продали 4,1 млн единиц маркированного средства. На втором месте – натрия хлорид. Казахстанцы купили 2,1 млн единиц. В тройку лидеров вошёл и парацетамол. Его приобрели 1,75 млн пачек».
На четвертом месте по продажам среди маркированных лекарственных средств – ацетилсалициловая кислота. Продано более 1,5 млн единиц. Пятерку замыкает нафазолин, сосудосуживающее средство, применяемое при насморке.
Кстати, год назад, список популярных лекарств в Казахстане был примерно таким же.
«Заметный спрос зафиксирован на Цитрамон П – более 1,23 млн единиц. В ТОП-10 также вошли меновазин – 897 тысяч, ТераФлю от гриппа и простуды, активированный уголь – 636 тысяч и фурациллин – 623 тысячи проданных лекарственных средств», – отмечают в Минздраве.
Между тем в Бюро нацстатистики 1 апреля 2026 года заявили, что несмотря на замедление инфляции, ряд товаров в стране продолжает дорожать. В том числе и некоторые лекарства. В списке – активированный уголь, который подорожал на 66,5%, парацетамол, который в лидерах у покупателей, прибавив 53,8% и ацетилсалициловая кислота. Последний препарат стал дороже на 52,2%.
При этом в Минздраве указали, что стоимость некоторых препаратов в марте снизилась в среднем на 25% благодаря тому, что в стране пересмотрели предельные цены на лекарства.
Механизм формирования предельных цен внедрил Комитет медицинского и фармацевтического контроля для снижения финансовой нагрузки на пациентов и исключения необоснованных наценок.
«В результате пересмотра цен изменения коснулись около пяти тысяч наименований лекарственных препаратов, реализуемых в розничной сети. В перечень вошли медикаменты для лечения хронических заболеваний сердечно-сосудистой системы, органов дыхания, инфекционных и других распространенных заболеваний. В настоящее время предельные цены установлены на 4994 торговых наименования», – говорится в сообщении.
В Минздраве подчеркнули, что аптеки и другие субъекты фармацевтической деятельности обязаны продавать лекарства по ценам, не превышающим установленный предельный уровень.
О фактах завышения стоимости препаратов граждан просили сообщить через мобильное приложение DariKZ или в региональные департаменты Комитета медицинского и фармацевтического контроля.
Напомним, в Казахстане планируют до конца 2026 года зарегистрировать новый препарат против онкологических заболеваний DVC. Об этом на брифинге в правительстве рассказал министр науки и высшего образования Саясат Нурбек.
По его словам, разработка, которой занимается национальная лаборатория Астаны, сейчас проходит дополнительные клинические испытания. Подробнее об этом читайте здесь.
Подписывайтесь на официальный Telegram-канал CMN.KZ